三溴化磷
三溴化磷为淡黃色發煙無色液體,有刺激性臭味,具腐蝕性。可溶於丙酮、二硫化碳、氯仿、四氯化碳。目前用於化學分析和有机合成,或作為催化劑。
| 三溴化磷 | |
|---|---|
 | |
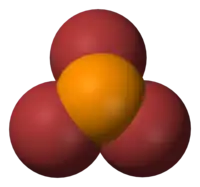 | |
| IUPAC名 phosphorus tribromide | |
| 别名 | 溴化磷(III) |
| 识别 | |
| CAS号 | 7789-60-8 |
| PubChem | 24614 |
| ChemSpider | 23016 |
| SMILES |
|
| EINECS | 232-178-2 |
| RTECS | TH4460000 |
| 性质 | |
| 化学式 | PBr3 |
| 270.70 g·mol⁻¹ | |
| 外观 | 无色清澈液体 |
| 密度 | 2.852 g/cm3 (液) |
| 熔点 | -41.5 °C (231.7 K) |
| 沸点 | 173.2 °C (446.4 K) |
| 溶解性(水) | 迅速水解 |
| 结构 | |
| 分子构型 | 三角锥 |
| 危险性 | |
| 警示术语 | R:R14, R34, R37 |
| 安全术语 | S:S25, S45 |
| 主要危害 | 腐蚀性,有毒 与水和醇反应 |
| 相关物质 | |
| 其他阴离子 | 三氟化磷、三氯化磷 三碘化磷 |
| 其他阳离子 | 三溴化氮、三溴化砷 三溴化锑 |
| 相关化学品 | 五溴化磷、溴氧化磷 七溴化磷 |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
三溴化磷對眼睛、皮膚、粘膜和呼吸道有強烈的刺激性。人體經呼吸吸入、誤食或皮膚接觸後,會產生燒灼感、咳嗽、喘息、喉炎、氣短、頭痛、恶心和嘔吐。
反应及有机合成应用
三溴化磷与水反应,生成溴化氢和亚磷酸,反应激烈时会发生爆炸:
- PBr3 + 3 H2O → H3PO3 + 3 HBr
三溴化磷和三氯化磷、三氟化磷类似,都可作为路易斯酸或路易斯碱。一方面,它可与三溴化硼生成1:1加合物Br3B-PBr3;另一方面,它也可作为亲电试剂与胺反应。
PBr3最常用作转化醇为溴代烃,分子中的三个溴原子都可溴化:[1]
机理涉及SN2亲核取代反应,如下图所示:
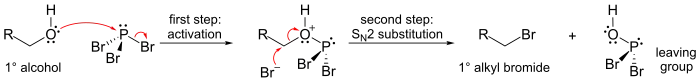
由于机理的缘故,该反应只对一级和二级醇起作用,而且反应后α碳发生构型翻转。
三溴化磷也可用作羧酸α氢溴化反应中的催化剂,制取Hell-Volhard-Zelinsky反应反应物酰溴的前体[2] 以及合成药物等。
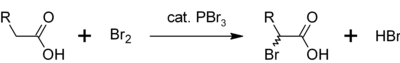
参考资料
- Greenwood, N. N.; Earnshaw, A. (1997). Chemistry of the Elements, 2nd Edition, Oxford:Butterworth-Heinemann. ISBN 0-7506-3365-4.
- J. March, Advanced Organic Chemistry, 4th ed., p. 723, Wiley, New York, 1992.
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.