烯丙醇
烯丙醇,丙烯的3位被羟基取代后得到的醇衍生物,即3-丙烯醇,结构为CH2=CH-CH2-OH。广义的烯丙醇泛指带双键的醇,同时双键和羟基的相对位置满足3-丙烯醇的结构。
| 烯丙醇 | |
|---|---|
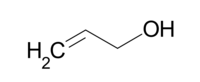 | |
| IUPAC名 Prop-2-en-1-ol Allyl alcohol | |
| 识别 | |
| CAS号 | 107-18-6 |
| PubChem | 7858 |
| ChemSpider | 13872989 |
| SMILES |
|
| InChI |
|
| InChIKey | XXROGKLTLUQVRX-UHFFFAOYAC |
| ChEBI | 16605 |
| KEGG | C02001 |
| 性质 | |
| 密度 | 0.854 g/ml |
| 熔点 | −129 °C |
| 沸点 | 97 °C |
| 溶解性(水) | 可溶 |
| 危险性 | |
欧盟危险性符号 有毒 T 有毒 T 危害环境N 危害环境N | |
| 警示术语 | R:R10-R23/24/25-R36/37/38-R50 |
| 安全术语 | S:S1/2-S36/37/39-S38-S45-S61 |
| 欧盟编号 | 603-015-00-6 |
| NFPA 704 |
 3
3
0
|
| 闪点 | 21 °C |
| 自燃温度 | 378 °C |
| 爆炸極限 | 2.5–18.0% |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
制备
烯丙醇可以使用多种方法获得。[1] 传统路线是烯丙基氯的水解:
- CH2=CHCH2Cl + NaOH → CH2=CHCH2OH + NaCl
烯丙醇也可由环氧丙烷的重排反应得到,反应需要在高温下由明矾催化。这一路线与烯丙基氯路线相关,好处是不会生成氯化钠。另一种不生成含氯中间体的方法是将丙烯乙酰氧基化为乙酸烯丙酯:
- CH2=CHCH3 + 1/2 O2 + CH3CO2H → CH2CHCH2O2CCH3 + H2O
参考文献
- Ludger Krähling, Jürgen Krey, Gerald Jakobson, Johann Grolig, Leopold Miksche “Allyl Compounds” Ullmann's Encyclopedia of Industrial Chemistry 2002, Wiley-VCH, Weinheim. doi:10.1002/14356007.a01_425
- Oliver Kamm and C. S. Marvel (1941). "Allyl alcohol". Org. Synth.; Coll. Vol. 1: 42.
外部链接
- 国际化学品安全卡0095
- NIOSH Pocket Guide to Chemical Hazards. . NIOSH.
- Institut national de recherche et de sécurité (2004). "Alcool allylique."PDF Fiche toxicologique n° 156. Paris:INRS. (法文)
- State of Michigan public information on allyl alcohol (页面存档备份,存于)
- Occupational exposure guidelines
- Datasheet regulatory information (页面存档备份,存于)
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.